目的
慢性腎臓病(CKD)は年々患者数が増えており,国の施策として「腎疾患対策検討会」において我が国における腎疾患対策のあり方について検討し、「腎機能異常の重症化を防止し、慢性腎不全による透析導入への進行を阻止すること」、及び「慢性腎臓病(CKD) に伴う循環器系疾患(脳血管疾患、心筋梗塞等)の発症を抑制すること」を目標として 腎疾患対策の方向性が示されている.
今回慢性腎臓病モデルとして利用されているアデニンを混餌で投与することによりマウスのCKDモデルを作製した.
方法
マウス,C57BL/6J,雄
8週齢
正常粉末飼料(CE-2),アデニン0.1%含有粉末飼料,アデニン0.2%含有粉末飼料
各群6例
マウスに正常粉末飼料を与える群とアデニンを0.1或いは0.2%混ぜ合わせた粉末飼料を与える群を設けた.粉末飼料は28日間与え,採血はアデニン投与開始前,その後1週間ごとに4回無麻酔下で頚静脈(鎖骨下静脈)より実施した.血液は遠心分離後血漿(ヘパリン)を採取し,BUN,Creを経時的に測定した.28日間アデニン食を与えた後,0.2%アデニン群は正常食に変更後,更に血中パラメーターの測定を行った.
結果
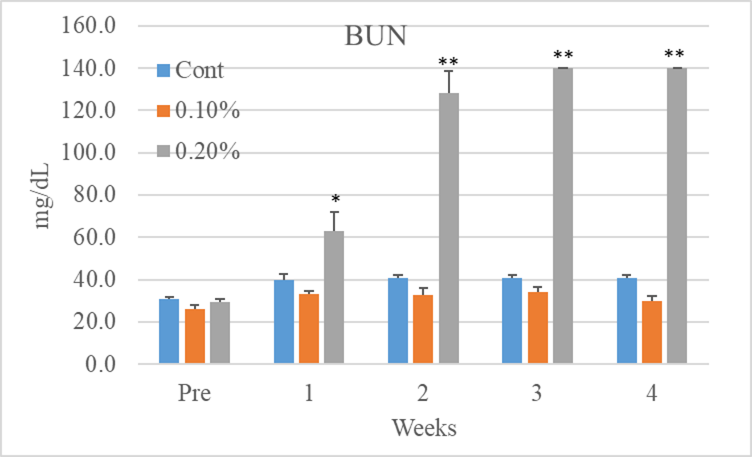
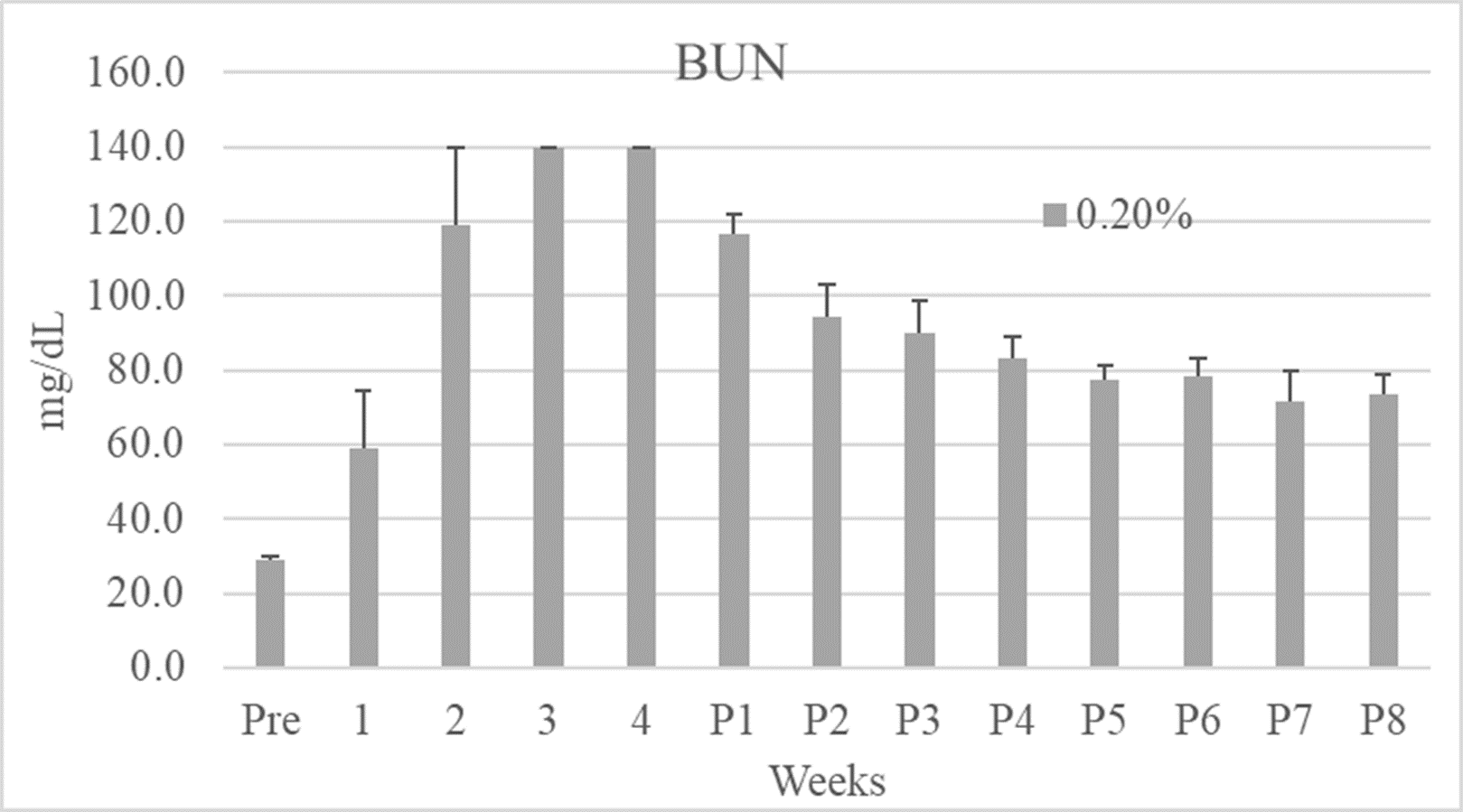
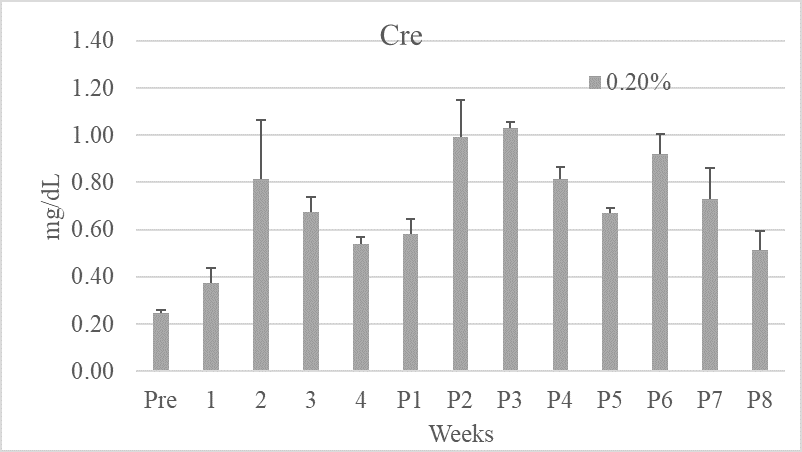
正常食群及び0.1%アデニン投与群では体重,血中パレメーターともに28日間で影響は認められなかった.しかし,0.2%アデニン群では体重は投与開始1週目から有意な減少が認められ,4週目まで減少し続けた.また,開始後2週目では0.2%アデニン食群の床敷きの汚れが目立ち,尿量が増加している様子が伺われ,その傾向は4週目まで認められた.また,腎障害の血中パラメーターであるBUNは投与開始後1週目から有意な上昇が認められ,4週目まで継続した.CreはBUNと異なり,投与開始後2週目で増加のピークに達し,以後漸次減少したが,4週目までは対照群と比較し有意に高値であった.この結果から0.2%のアデニン投与によりCKDモデルの作製は可能であるが,その影響は強すぎることが示された.
図1 体重変化
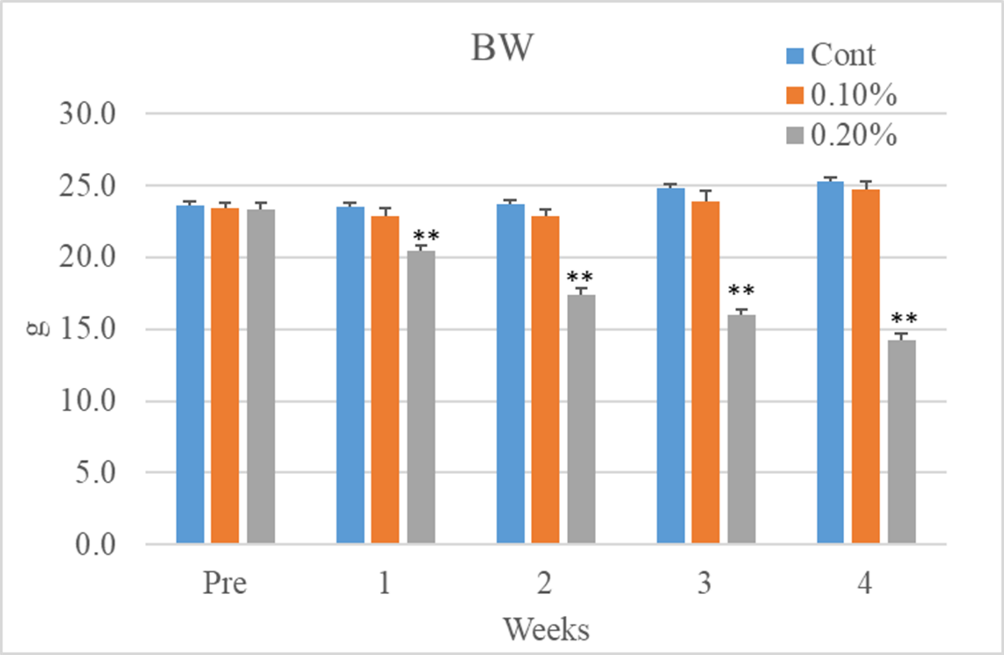
図2 BUN,Cre
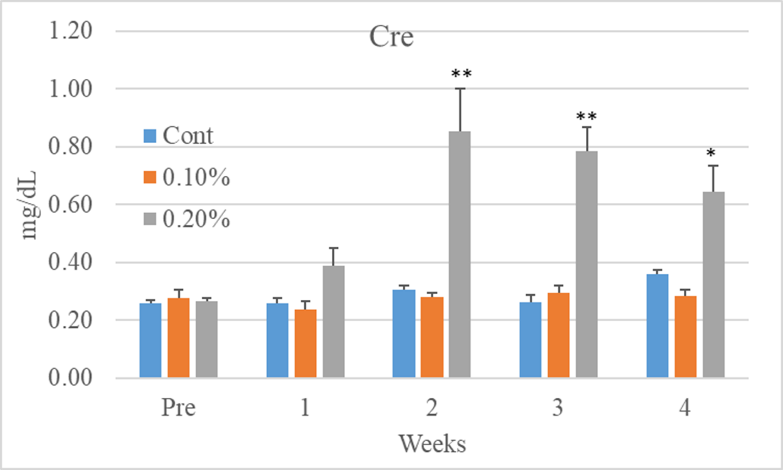
Creの減少が体重に影響されていると判断されたことから,0.2%アデニン群に関しては餌を正常食に変更し,体重,BUN,Creを週1回測定し,8週目まで実施した.その結果,アデニン投与を中止することにより,体重は増加し,BUNは減少することが示された.これだけであればCKDの病態が軽減されているように見えるが,Creは増加することから,CKDの病態が軽減しているのではなく,安定した病態を示していることを表している.
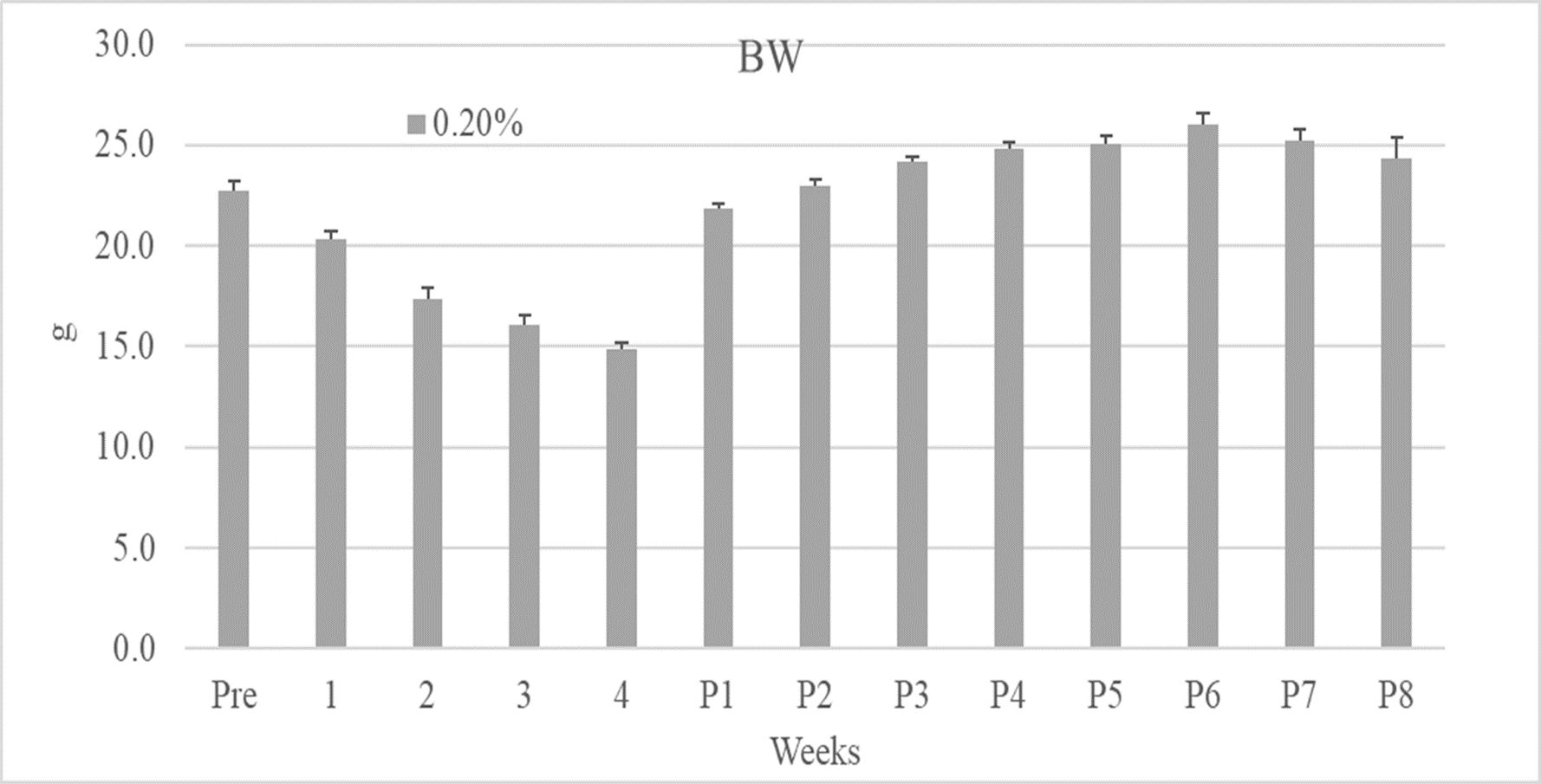
まとめ
アデニンを混餌することにより,ラット同様慢性腎不全モデルを作製することが出来た.しかし,0.1%では全く影響がなく0.2%では体重の減少を引き起こすほどの強度なCKDモデルであることが示されている.この変化はこれまでの報告と一致しているが,血中パラメーターの経時的報告はなく,Creの増加が徐々に増加するのではなく,2週目でピークを迎え,その後減少することは今までに報告はなされていない.Creは筋肉から分泌される物質であり,体重(筋肉)が減少することにより,分泌量が下がるため,体重低下に対して血中Cre量が下がるのは当然の結果である.
そのため,Creの上昇に関して4週目で薬効評価を行った場合,正確な評価を行えていない可能性を示している.4週目の結果のみで評価した場合,体重との関係を評価する必要がある.また,単純に体重換算しても体重の増加がすぐにCreの値に影響を及ぼしていない.そのため,正しく薬効を評価されていない可能性がある.
今回の結果から,0.2%濃度のアデニンを用いてCKDに対する薬効評価を行うには,4週間のアデニン投与によりCKDモデルを作製し,その後正常食に変更後2週目から被験物質の投与を実施することが,薬効を評価するには適していると考えられる.
自社開発技術の紹介
小動物
慢性腎不全モデルラットの作製
-腎動脈分枝結紮法-
マウスを用いた耐糖能試験
-OGTT-
坐骨神経切除による腓腹筋,
ヒラメ筋,足底筋に対する影響
慢性腎不全モデルラットの作製
-アデニン誘発慢性腎不全モデル-
デキストラン硫酸ナトリウム誘発
潰瘍性大腸炎モデルの作製
マウスの無麻酔経時採血方法の検討
‐頚静脈(鎖骨下静脈)‐
経口脂質負荷試験(OLTT)を用いて
新規肥満・糖尿病マウス作製法を用いた
肥満・糖尿病予防効果(特許出願中)
新規肥満・糖尿病マウスの作製(特許出願中)
慢性腎不全モデルマウスの作製
‐アデニン誘発慢性腎不全モデル(1)‐
慢性腎不全モデルマウスの作製
‐アデニン誘発慢性腎不全モデル(2)‐
大動物
低用量STZ誘発性糖尿病
モデルブタの作製

 CONTACT
CONTACT
お仕事のご依頼、詳しい内容のご相談などをご希望の場合はお問合せフォームからお気軽にご連絡ください。

 お問合せ
お問合せ